
Chelat-bildende Modifikationen
DTPA
DTPA-modifizierte Oligonucleotide
Diethylentriaminpentaessigsäure (DTPA), auch bekannt als Pentetsäure ist ein Chelatbildner, der äußerst stabile Komplexe mit Metallsalzen eingehen kann. DTPA ist eine Aminopolycarbonsäure, die sich aus einem Diethylentriamin-Rückgrat mit fünf Carboxymethylgruppen zusammensetzt.
DTPA hat eine starke Affinität zu Metallkationen mit großem Ionenradius. Neben verschiedenen Schwermetallionen können hierbei auch die etwas kleineren Eisenionen effizient gebunden werden. Unter der Annahme, dass jedes Stickstoffatom und jede Carboxylgruppe als potenzieller Koordinationsbindungspartner fungieren kann, verfügt das Pentaanion DTPA5- über bis zu acht freie Bindungsstellen. Dabei wickelt sich DTPA regelrecht um das Metallion. Da bei manchen Komplexen mit bestimmten Metallen weniger Koordinationsstellen benötigt werden, kann DTPA auch nach Komplexierung eines Metalls über die verbliebenen freien Reaktionsseiten weitere Reaktionspartner an sich binden.
Chelate, bestehend aus Gadolinium-Ionen (Gd3+) und DTPA bilden äußerst starke Komplexe, die auch intrazellulär Anwendung finden. So werden beispielsweise DTPA-komplexierte Gd-Ionen als Kontrastmittel in der Magnetresonanztomografie (MRT) eingesetzt, um den Kontrast in der Bildgebung zu verstärken.
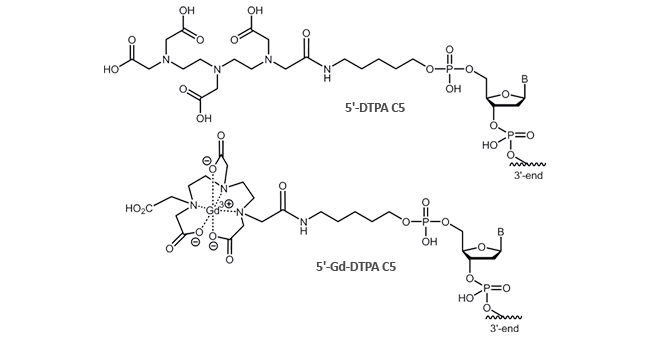
DTPA kann an den 5´-Terminus des Oligonucleotids gebunden werden. Aktuell ist die Modifikation an Oligos bis zu einer Länge von 45 Basen möglich.
Literatur:
1. Gadolinium(III) Complexes with N-Alkyl-N-methylglucamine Surfactants Incorporated into Liposomes as Potential MRI Contrast Agents. Silva RS, Correia Duarte E, Ramos GS, Kock FVC, Diuk Andrade F, Frézard F, Colnago LA, Demicheli C; Bioinorganic Chemistry and Applications (2015), Volume 2015, Article ID 942147, 8 pages.
2. Characteristics of gadolinium-DTPA complex: a potential NMR contrast agent. Weinmann HJ, Brasch RC, Press WR, Wesbey GE. AJR Am J Roentgenol. (1984); 142(3):619-24.
3. Gadolinium-DTPA as a contrast agent in MRI: initial clinical experience in 20 patients. Carr DH, Brown J, Bydder GM, Steiner RE, Weinmann HJ, Speck U, Hall AS, Young IR; American Journal of Roentgenology. (1984); 143: 215-224. 10.2214/ajr.143.2.215.
4. Molecular MR Contrast Agents for the Detection of Cancer: Past and Present. Bogdanov A, Mazzanti ML; Semin Oncol. (2011); 38(1): 42–54.
5. Macromolecular MRI contrast agents: Structures, properties and applications. Tang J, Sheng Y, Hu H, Shen Y; Progress in Polymer Science (2013); Volume 38, Issues 3–4, Pages 462-502.
DOTA
DOTA-modifizierte Oligonucleotide
DOTA (1,4,7,10-Tetraazacyclododecan-1,4,7,10-tetraessigsäure) enthält vier Essigsäurecarboxylatgruppen an den vier Stickstoffatomen seiner zwölfatomigen zyklischen Struktur. Ähnlich dem DTPA ist auch DOTA in der Lage zwei- und dreiwertige Metallionen (z.B. Gadolinium Gd3+) zu binden und mit ihnen stabile Chelatkomplexe auszubilden. Über eine der bis zu acht Bindungsstellen kann DOTA nach Komplexierung eines Metallions auch Proteine und andere Biomoleküle (Antikörper, Peptide, Biotin etc.) kovalent binden.
Aufgrund seiner hohen in vivo und in vitro Stabilität findet DOTA in Kombination mit komplexierten Gd-Ionen wie DTPA als chelatisierender Komplexbildner als Kontrastmittel in der Magnetresonanztomografie (MRT) Anwendung.
Der Chelatbildner DOTA ist als 5´-Modifikation am Oligonucleotid verfügbar. DOTA wird hierbei mithilfe des clickreaktiven DBCO an das Oligo gebunden.
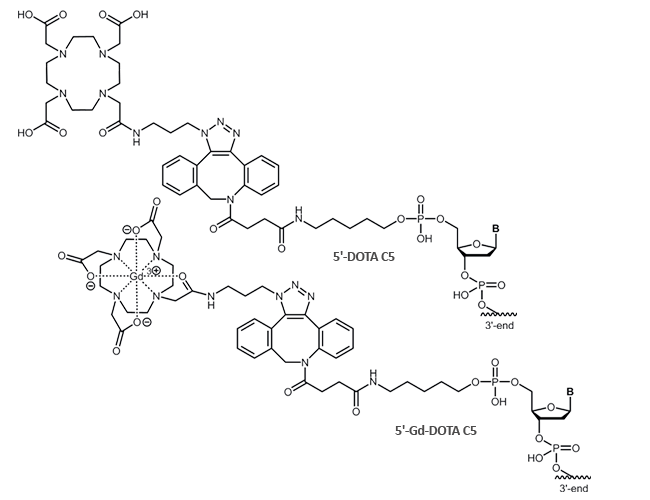
Literatur:
1. Labeling of Oligonucleotides with DTPA and DOTA on Solid Phase. Hovinen J; Nucleosides, Nucleotides and Nucleic Acids (2007), Volume 26, Issue 10-12.
2. Solid-phase oligonucleotide labeling with DOTA. Jaakkola L, Ylikoski A, Hovinen J; Curr Protoc Nucleic Acid Chem. (2007), Chapter 14:Unit 4.31. doi: 10.1002/0471142700.nc0431s29.
3. Isomerism in benzyl-DOTA derived bifunctional chelators: implications for molecular imaging. Payne KM, Woods M; Bioconjug Chem. (2015), 26(2):338-44. doi: 10.1021/bc500593h.
4. Synthesis of a gadolinium basedmacrocyclic MRI contrast agent for effective cancer diagnosis. Jeong Y, Na K; Biomaterials Research (2018) 22:17, doi.org/10.1186/s40824-018-0127-9.
5. Pre-targeted radioimmunotherapy of human colon cancer xenografts in athymic mice using streptavidin-CC49 monoclonal antibody and 90Y-DOTA-biotin. Domingo RJ, Reilly RM; Nuclear Medicine Communications (2000), 21(1):89-96.
NTA
NTA-Oligo-Konjugate
Ein weiterer Vertreter der Chelatbildner ist die Nitrilotriessigsäure (NTA). NTA zeigt nach Komplexierung zweiwertiger Metallionen (Ni2+, Cu2+, etc.) eine hohe Affinität zu Polyhistidin-markierten Molekülen
(z.B. rekombinante Proteine) und bindet diese sehr effizient. Vor allem aus dem Bereich der Reinigung und Isolierung rekombinanter Proteine (Metallaffinitätschromatografie) ist diese Eigenschaft des Chelatbildners NTA bekannt.
Gekoppelt an ein DNA-Oligonucleotid kann die Eigenschaft der His-Tag-Bindung genutzt werden, um beispielsweise DNA-Protein-Konjugate auszubilden.
NTA wird als 5´- oder 3'-Modifikation über ein entsprechendes Azid kupferfrei an ein DBCO-modifizietes Oligo geclickt.
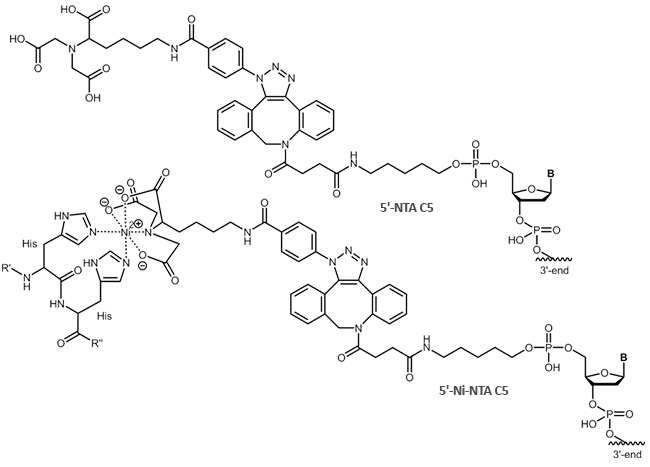
Literatur:
1. Conjugation of DNA with protein using His-tag chemistry and its application to the aptamer-based detection system. Shimada J, Maruyama T, Hosogi T, Tominaga J, Kamiya N, Goto M; Biotechnology Letters (2008), Volume 30, Issue 11, pp 2001–2006.
2. Oligohis-tags: mechanisms of binding to Ni2+-NTA surfaces. Knecht S, Ricklin D, Eberle AN, Ernst B; J Mol Recognit. (2009); 22(4):270-9. doi: 10.1002/jmr.941.
3. DNA-enzyme conjugate with a weak inhibitor that can specifically detect thrombin in a homogeneous medium. Shimada J, Maruyama T, Kitaoka M, Kamiya N, Goto M; Anal Biochem. (2011), 414(1):103-8. doi: 10.1016/j.ab.2011.02.035.

