
Lipophile Modifikationen
Durch das Ribose-Phosphat Rückgrat sind einfache Oligonucleotide hydrophil und gut in Wasser oder Puffer löslich. Mit der Koppelung einer lipophilen Modifikation wird die Löslichkeit verändert, das Oligo erhält amphiphilen Charakter und kann so auch mit den hydrophoben Phasen in Membranen, Fette oder Proteine interagieren. Durch die lipophile Gruppe ist ein erhöhter Transport durch Membranen und somit eine verbesserte Aufnahme in Zellen und Gewebe möglich, ein z. B. für die Wirkstoffforschung wichtiger Aspekt. Die Wirksamkeit der verschiedenen lipophilen Modifikationen wurde für Antisense, siRNA, Aptamer und Immuno-stimulatorische Oligos geprüft. Auch in der Nanobiotechnologie finden sie Verwendung.
| Modifikation | 5´ | 3´ |
|---|---|---|
| Cholesterol | x | x |
| α-Tocopherol | x | |
| Trolox | x | x |
| Palmitat | x | |
| Stearat | x | |
| Distearoyl-Lipid | x | |
| Ibuprofen | x | x |
Cholesterol
Cholesterol
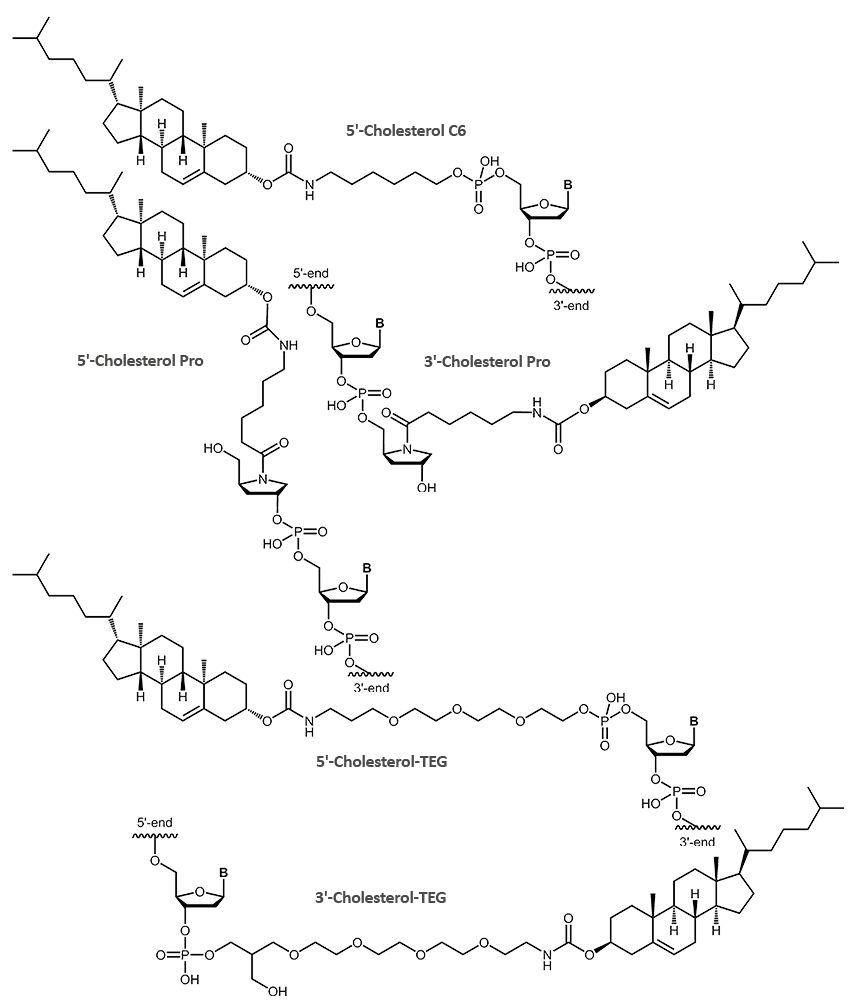
Verbesserter Transport und erhöhte Aufnahme wurde für DNA-Antisense-Oligos und siRNAs gezeigt. Der stark lipophile Charakter des Steroids Cholesterols ermöglicht deutlich höhere Aufnahmen in die Zellen und damit verbunden die höhere Wirksamkeit Cholesterol-modifizierter Oligonucleotide.
Die hydrophobe Eigenschaft des Cholesterols kann auch dazu genutzt werden, Oligonucleotid-Konjugate in Membranen oder Vesikeln zu verankern. Ein Ansatz, mit dem u.a. artifizielle DNA-Nanostrukturen an Lipidmembranen gebunden werden können.
 |
Literatur:
1. Modification of antisense phosphodiester oligodeoxynucleotides by a 5' cholesteryl moiety increases cellular association and improves efficacy. Krieg AM, Tonkinson J, Matson S, Zhao Q, Saxon M, Zhang LM, Bhanja U, Yakubov L, Stein CA; Proc. Natl. Acad. Sci USA (1993), 90, 1048-1052.
2. Silencing of microRNAs in vivo with ‘antagomirs‘. Krützfeldt J, Rajewsky N, Braich R, Rajeev KG, Tuschl T, Manoharan M, Stoffel M; Nature (2005), 438, 685 - 689.
3. Synthetic lipid membrane channels formed by designed DNA nanostructures. Langecker M, Arnaut V, Martin TG, List J, Renner S, Mayer M, Dietz H, Simmel FC; Science (2012), 338. 932 – 936.
Tocopherol, Trolox
Tocopherol, Trolox
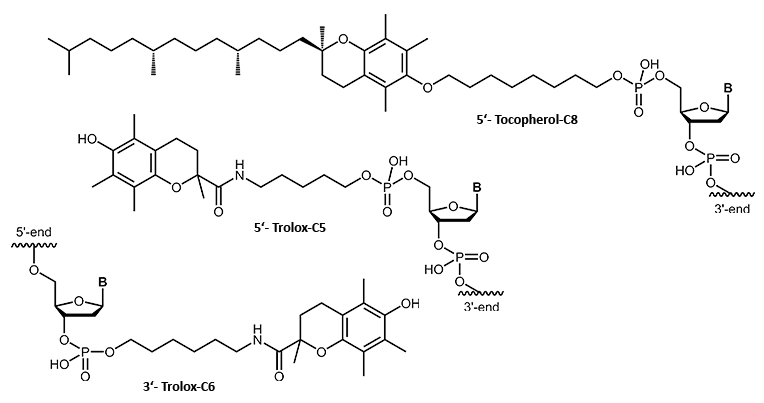
α-Tocopherol ist ein natürlich vorkommendes Vitamin (Vitamin E Gruppe). An Oligonucleotide konjugiert, verleiht es dem Konjugat einen amphiphilen Charakter. Tocopherol wird im Körper durch spezifische Proteine und Carrier transportiert, die auch für den Transport der Oligo-Konjugate genutzt werden können.
Als Tocopherol-Derivat gehört Trolox ebenfalls in die Vitamin E Gruppe. Im Vergleich zu Tocopherol verfügt Trolox jedoch über hydrophilere Eigenschaften und zeigt des Weiteren einen ausgeprägten antioxidativen Charakter. Durch die verbesserte interzelluläre Wirkung und Aufnahme in die Zelle ergeben sich für Oligo-Konjugate mit diesen lipophilen Modifikationen optimale Einsatzmöglichkeiten im Bereich der Antisense-Oligonucleotide.
In Kombination mit einem Farbstoff ist Trolox in der Lage den Farbstoff zu "stabilisieren" und gegen Ausbleichen zu schützen.
 |
Literatur:
1. Efficient in vivo delivery of siRNA to the liver by conjugation of alpha-tocopherol. Nishina K, Unno T, Uno Y, Kubodera T, Kanouchi T, Mizusawa H, Yokota T; Mol Ther. (2008), 16:734–740.
Stearat, Palmitat, Distearoyl-Lipid
Stearat, Palmitat, Distearoyl-Lipid
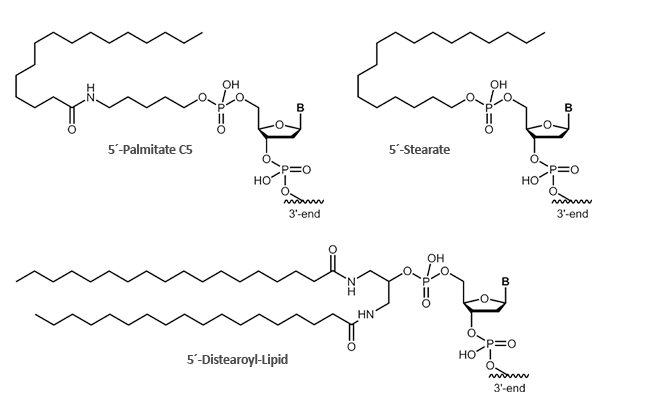
Durch das Ankoppeln einer Fettsäure an ein Oligo erhält das Konjugat einen hydrophoben Charakter und kann an Lipidphasen, Doppelmembranen oder Vesikel binden. Das Oligo bleibt dabei zur wässrigen Phase hin orientiert, während die Fettsäure in die Lipidphase eintaucht. Eine erhöhte Aufnahme durch Zellmembranen wird ebenfalls beobachtet.
Bei biomers.net erhalten Sie verschiedene Fettsäuren:
- Palmitat
- Stearat
- Distearoyl-Lipid
 |
Literatur:
1. DNA modification of live cell surface. Borisenko GG, Zaitseva MA, Chuvilin AN, Pozmogova GE; Nucleic Acids Res. (2009), 37, e28.
2. Lipid modification of GRN163, an N3' -> P5' thio-phosphoramidate oligonucleotide, enhances the potency of telomerase inhibition. Herbert BS, Gellert GC, Hochreiter A, Pongracz K, Wright WE, Zielinska D, Chin AC, Harley CB, Shay JW, Gryaznov SM; Oncogene (2005), 24, 5262–5268.
3. General method for modification of liposomes for encoded assembly on supported bilayers. Yohina-Ishii, Miller GP, Kraft ML, Kool ET, Boxer SG; J. Am. Chem. Soc. (2005), 9, 1356- 1357.
Ibuprofen
Antisense Oligonucleotide und Aptamere mit Ibuprofen
Die Kopplung kleiner Moleküle wie Ibuprofen an ein DNA-Oligonucleotid stellt einen neuen Ansatz dar, die Lebensdauer von Aptameren in der Zelle deutlich zu erhöhen.
Enzymatische Degradation durch Endo- und Exonucleasen, sowie die Bereinigung vergleichsweise kleiner Moleküle wie Aptamere und Antisense Oligonucleotide (25-30 kDa) aus dem Kreislauf durch Niere und Leber limitieren die intrazelluläre Lebensdauer dieser möglichen Wirkstoffe und reduzieren somit auch deren therapeutisches Potenzial.
Stoffe wie Ibuprofen können am Albumin oder andere Serumproteine binden, ebenso wie Ibuprofen-Konjugate (z.B. Oligonucleotide, die chemisch mit Ibuprofen verknüpft wurden).3
Aufgrund der erhöhten Molekulargewichte dieser Komplexe (Antisense Oligonucleotid / Aptamer-Ibuprofen-Albumin) wird die Beseitigung durch Leber und Niere aus dem Kreislauf erschwert und die Resistenz gegen enzymatischen Abbau (Endo- und Exonucleasen) erhöht.1,2
Auf diese Weise kann die Lebensdauer sowie intrazelluläre Verteilung und damit die pharmakologische Verfügbarkeit der modifizierten Antisense Oligonucleotide bzw. Aptamere verbessert werden.2 Am Zielort kann sich das Oligonucleotid-Ibuprofen-Konjugat vom Albumin-Träger lösen und gegebenenfalls seine Wirkung entfalten.2
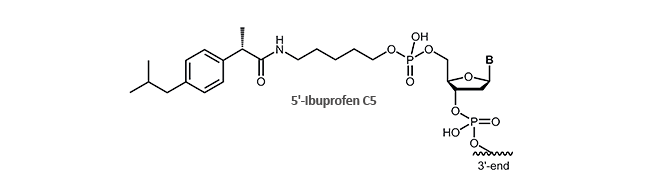
Ab sofort bietet biomers.net Ibuprofen als 5´-und /oder 3´- Modifikation für DNA-Oligonucleotide an.
Literatur:
1. Predicting the Uncertain Future of Aptamer-Based Diagnostics and Therapeutics. Bruno, JG; Molecules (2015), 20, 6866-6887; doi:10.3390/molecules20046866.
2. A Review of Therapeutic Aptamer Conjugates with Emphasis on New Approaches. Bruno, JG; Pharmaceuticals (2013), 6, 340-357; doi:10.3390/ph6030340.
3. Improving Antisense Oligonucleotide Binding to Human Serum Albumin: Dramatic Effect of Ibuprofen Conjugation. Manoharan M, Inamati GB, Lesnik EA, Sioufi NB, Freier SM; Chembiochem. (2002); 3(12):1257-60.

